
Выбор тактики лечения пациентов детского возраста с синдромом Гийена—Барре с учетом фармакоэкономического анализа
Журнал: Журнал неврологии и психиатрии им. С.С. Корсакова. 2018;118(3): 39‑45
Прочитано: 1547 раз
Как цитировать:
В 1916 г., более 100 лет назад, врачи G. Guillain, J.-A. Barré и A. Strohl опубликовали данные о новом заболевании, протекающем в виде острого вялого тетрапареза, которое было названо синдромом Гийена—Барре (СГБ). С того времени прояснились многие особенности этой патологии. Известно, что СГБ — острая воспалительная аутоиммунная полирадикулонейропатия с очерченной клинической картиной: остро возникающей прогрессирующей мышечной слабостью в конечностях, снижением или полным угнетением сухожильных рефлексов, развитием белково-клеточной диссоциации в цереброспинальной жидкости (ЦСЖ). Как правило, заболевание имеет доброкачественное течение. Несмотря на существенный прогресс в изучении СГБ, остается ряд нерешенных вопросов, в том числе о наиболее эффективной схеме лечения заболевания [1].
В настоящее время СГБ является ведущей причиной острых вялых параличей: в мире в год регистрируется примерно 100 000 случаев заболевания среди детей и взрослых, или от 0,38 до 2,53 случая на 100 000 населения [2, 3]. Работ по анализу течения СГБ в детской популяции довольно мало. По их данным, распространенность СГБ среди детей европейского региона в возрасте 0—15 лет составляет 0,34—1,34 случая на 100 000 населения в год [4, 5]. Результаты ретроспективного анализа особенностей течения СГБ у детей в Московском регионе показали сопоставимые результаты [6]. Ранее основной причиной развития вялых параличей у детей и взрослых являлась паралитическая форма полиовирусной инфекции. Успехи глобальной инициативы ВОЗ по ликвидации полиомиелита привели к существенному сокращению числа таких случаев [5]. Наряду с этим в Российской Федерации (РФ) и некоторых странах Европы осуществляется эпидемиологический надзор за всеми случаями острых вялых параличей у детей до 15 лет, благодаря чему формируется единый реестр пациентов с СГБ. Особое внимание привлекла выявленная в последние годы ассоциация СГБ с заболеванием, вызванным вирусом Зика. Недавний всплеск этой инфекции на территориях стран Латинской Америки и Карибского бассейна внес существенные изменения в представления о заболеваемости СГБ: независимый анализ показал, что эти два заболевания ассоциированы [7]. На каждую 1000 случаев заболевания вирусом Зика пришлось порядка 0,24 случая СГБ [8, 9]. Кроме того, была показана ассоциация заболеваемости СГБ с другими флавивирусами. Случаи СГБ, ассоциированные с вирусом Зика, внесли существенный вклад в повышение показателя заболеваемости. Так, выявление СГБ в мире с 2015 г. увеличилось в 2—9,8 раза [10]. Этот факт диктует необходимость дальнейшего поиска и изучения вероятных пусковых механизмов СГБ.
Патогенез СГБ, вероятнее всего, различается в зависимости от формы заболевания. Предполагается, что антитело-опосредованный и Т-клеточный механизмы дополняют друг друга и усугубляют повреждение нервного волокна [1, 3, 11, 12]. При нарушении целостности последнего вследствие аутоиммунной атаки ухудшается проводимость импульса по нервам, что и приводит к развитию вялого паралича.
Существует несколько общепринятых схем терапии СГБ у детей, и выбор подхода зависит от практики конкретного лечебного учреждения. В статье приводятся данные о наиболее распространенных схемах терапии (применение курсов высокодозного внутривенного иммуноглобулина — ВВИГ и плазмафереза) и фармакоэкономический анализ прямых затрат на терапию СГБ у детей в РФ.
Три основные формы СГБ различаются по мишени поражения: две аксональные формы (острая моторная и острая моторно-сенсорная аксональные нейропатии) и острая воспалительная демиелинизирующая полинейропатия с поражением миелина. Эти формы имеют разную тяжесть течения и скорость нарастания парезов, варьируя от легкого поражения до тяжелых форм с развитием бульбарного синдрома и необходимостью оказания вентиляционной поддержки. При поздней диагностике и отсутствии адекватной терапии изменения могут носить необратимый характер [12].
Отличительной клинической чертой заболевания является острая прогрессирующая слабость в конечностях, иногда с вовлечением чувствительных волокон и поражением черепных нервов. Пик заболевания приходится на 2—4-ю неделю после предполагаемой активации иммунной системы. По данным исследования детской популяции Москвы [6], пик приходится на 1—2-ю неделю от начала заболевания: медиана достижения наиболее яркой клинической картины составила 9,5 [6,25; 12,5] сут от первых проявлений.
Согласно проведенному ранее исследованию во взрослой популяции РФ [12], тяжелое течение с развитием дыхательной недостаточности развивается у 19% больных. Во всех возрастных группах тяжелая форма СГБ встречается приблизительно в ¼ (20—30%) наблюдений [3]. Среди детей РФ наиболее распространенной является тяжелая форма заболевания, однако искусственная вентиляция легких необходима в небольшом числе случаев, что свидетельствует о редком вовлечении дыхательной мускулатуры [1, 3, 6, 13].
Наряду со своевременной диагностикой СГБ, ключевым моментом является правильно выбранная тактика терапии.
СГБ — заболевание, приводящее к временной инвалидизации, что требует комплексной терапии. Важны адекватная нутритивная поддержка, динамический контроль общего неврологического статуса с учетом вероятного развития бульбарного синдрома, постоянный мониторинг дыхательной функции и гемодинамических показателей, профилактика развития венозного тромбоза конечностей у обездвиженных пациентов. Ключевое место занимает патогенетическая иммунотропная терапия, к которой относятся высокообъемный программный плазмаферез и ВВИГ.
При СГБ недопустимо назначение глюкокортикостероидных препаратов: доказано, что этот вид иммуносупрессивной терапии абсолютно неэффективен. Такой подход в острый период заболевания вызывает эрозивно-язвенное поражение слизистой желудочно-кишечного тракта, что делает невозможным проведение плазмафереза. Также длительный пероральный прием глюкокортикостероидов у пациентов с СГБ способствует сохранению стойких остаточных явлений и развитию побочных эффектов [14].
По данным систематического обзора Cohrane, назначение глюкокортикостероидов в исследованиях не показало каких-либо положительных эффектов в сравнении с плацебо. Даже комбинирование ВВИГ с метилпреднизолоном не выявило более быстрого восстановления в сравнении с монотерапией ВВИГ. Несколько авторов приводят данные о более медленном восстановлении при применении глюкокортикостероидов [15, 16].
По данным обзора H. Willison и соавт. [3], оба терапевтических подхода (ВВИГ и плазмаферез) позволяют достичь более раннего наступления плато и добиться менее тяжелого течения заболевания, что было показано в крупных контролируемых рандомизированных исследованиях, проведенных в странах Европы и Северной Америки. Главной задачей врача является инициация лечения в наиболее ранние сроки — до момента наступления необратимого повреждения нервного волокна. Наиболее оправдана терапия, начатая в первые 2 нед заболевания [3, 17, 18].
Выбор между применением ВВИГ и плазмаферезом должен проводиться с учетом ряда особенностей. Применение ВВИГ имеет несколько практических преимуществ, к которым относятся более широкая доступность этого метода и отсутствие необходимости использования специализированного оборудования. Кроме того, ВВИГ сопровождается меньшим количеством осложнений. Главным противопоказанием к выбору ВВИГ в качестве первой линии терапии является указание в анамнезе на анафилактические реакции при применении иммунных препаратов [18].
Общепринятыми считаются две схемы терапии ВВИГ с суммарной дозировкой на курс 2 г/кг: 2-дневный курс с дозировкой 1 г/кг/сут или 5-дневный курс с дозировкой 0,4 г/кг/сут. Данных о преимуществах одного режима перед другим на настоящий момент не получено. Для уточнения информации об эффективности требуется проведение дополнительных исследований, однако в связи с развитием меньшего количества побочных эффектов и более редкой регистрацией терапийзависимых флюктуаций в течение заболевания более предпочтительной для детей считается 5-дневная схема терапии [4, 19].
Для лечения СГБ следует использовать исключительно препараты иммуноглобулина человека для внутривенного введения, содержащие не менее 95% иммуноглобулинов класса G (IgG). Предпочтительнее готовые к применению 10% растворы ВВИГ: их применение позволяет снизить волемическую нагрузку в 2 раза по сравнению с 5% растворами, что имеет решающее значение в педиатрической практике. Применение 10% растворов позволяет также существенно сократить длительность инфузии, что экономит время активного наблюдения медперсоналом. При выборе препаратов ВВИГ специалисты должны быть уверены в высокой степени очистки, патогенной безопасности и хорошей переносимости вводимого вещества. Технологии производства ВВИГ продолжают совершенствоваться, препараты последнего поколения обладают высокой степенью вирусной безопасности благодаря многоступенчатым методам очистки. В 2014 г. на российском рынке появился 10% раствор ВВИГ — препарат привиджен («CSL Behring», Швейцария). При его производстве используются современные методы очистки: 4 этапа инактивации и удаления вирусов, включая нанофильтрацию, а также анионобменная хроматография, применение которой позволяет достичь высокого содержания IgG (более 98%) и сохранить оптимальное распределение подклассов IgG, соответствующее плазме крови. Входящий в состав препарата привиджен стабилизатор L-пролин в сочетании с низким значением рН снижает содержание димеров IgG до требуемого уровня 12%, что способствует его лучшей переносимости и реже вызывает побочные действия [20].
Плазмаферез также ускоряет наступление периода восстановления, поэтому терапию лучше начинать в первую неделю заболевания. Однако эффект отмечается даже при старте терапии в течение первого месяца болезни. В настоящее время специальных стандартов проведения плазмафереза у детей с СГБ нет. Принято, что количество сеансов плазмафереза, во время которых происходит замещение одного объема плазмы, зависит от клинической картины: при легкой форме проводятся 2 сеанса, при средней — 4, при тяжелой — 6. Противопоказаниями к терапии плазмаферезом являются коагулопатии, сепсис, нестабильность гемодинамики и шоковое состояние [21—23]. При комбинировании двух методов терапии (курс ВВИГ после курса плазмафереза) более выраженного эффекта достигнуто не было [17]. В РФ существуют федеральные рекомендации по ведению пациентов с СГБ [14], в соответствии с которыми доказанной эффективностью обладает только высокообъемный программный плазмаферез, а проведение процедур плазмафереза дискретным методом является недопустимым. Данные о стоимости методов терапии сильно отличаются в зависимости от географического региона, как и их доступность.
К настоящему моменту данных о фармакоэкономике терапии СГБ у детей в России нет.
Цель настоящей работы — освещение актуальных данных о подходах к иммунотропной терапии на примере клинического случая с проведением фармакоэкономического анализа лечения.
Был проведен фармакоэкономический анализ прямых медицинских затрат для терапии СГБ у детей препаратами ВВИГ в сравнении с высокообъемным плазмаферезом. Расчет осуществляли на уровне отдельного лечебного учреждения, в котором проходят лечение больные с диагнозом СГБ младше 18 лет. В расчет включали только прямые медицинские затраты, что позволило отразить реальные расходы системы здравоохранения в рамках программы государственных гарантий на период нахождения пациента в стационаре.
Госпитализацию пациента можно условно разделить на 2 периода: первый, когда проводится патогенетическая терапия и медицинская помощь в острой фазе заболевания, и второй, когда проводятся реабилитационные мероприятия. Необходимость разделения оказываемой медицинской помощи на два этапа сопряжена с различной структурой затрат в указанные периоды. Средняя длительность госпитализации составила 27 дней для терапии ВВИГ и 41 день для терапии плазмафереза [6]. Длительность первого периода лечения, согласно рекомендациям [14], для ВВИГ составляет 5 дней, для плазмафереза — 10 дней. Далее более подробно будут рассмотрены затраты первого периода лечения, который сопряжен с основными расходами при каждом из подходов.
Высокая частота использования центральных венозных катетеров у детей обусловлена необходимостью многократных сеансов плазмафереза и эксфузии больших объемов крови. Основной вклад в совокупные затраты на процедуру плазмафереза вносят 3 типа затрат: на приобретение 5% раствора альбумина (37% затрат), расходных материалов (27%), а также на купирование осложнений (23%), другая небольшая часть затрат приходится на время медицинского персонала (11%) и аммортизационные отчисления (2%).
В связи с тем, что процедура предполагает удаление больших объемов плазмы, плазмозамещение необходимо проводить аналогичным количеством 5% раствора альбумина в соотношении 1:1. Объем замещаемой плазмы и оптимальное число процедур плазмафереза варьируют: возможно удаление плазмы в объеме от 140 до 250 мл/кг за 2-недельный курс лечения. Согласно протоколу, используемому в США, замещается 200—250 мл/кг в течение 7—10 дней [14]. В настоящем исследовании использовался объем заменяемой плазмы 250 мл/кг в течение 5 дней. При проведении расчетов на среднюю массу тела ребенка, равную 30 кг, необходимо удалить 6000—7500 мл в течение всего лечения. Затраты на альбумин рассчитывались исходя из стоимости 1 мл альбумина человека, равной 10,36 рубля.
При расчете затрат на расходные материалы учитывалась стоимость центрального венозного катетера и материалов, необходимых для проведения процедуры (кровопроводящие магистрали, гемосорбент, антикоагулянт).
Все осложнения процедуры можно разделить на 2 вида: осложнения, связанные с постановкой центрального венозного катетера, и осложнения, ассоциированные с процедурой плазмафереза. В крупном систематическом обзоре [24], в который были включены 74 исследования по анализу осложнений вследствие использования центрального венозного доступа в детской популяции, были зафиксированы серьезные осложнения при проведении плазмафереза (табл. 1). 
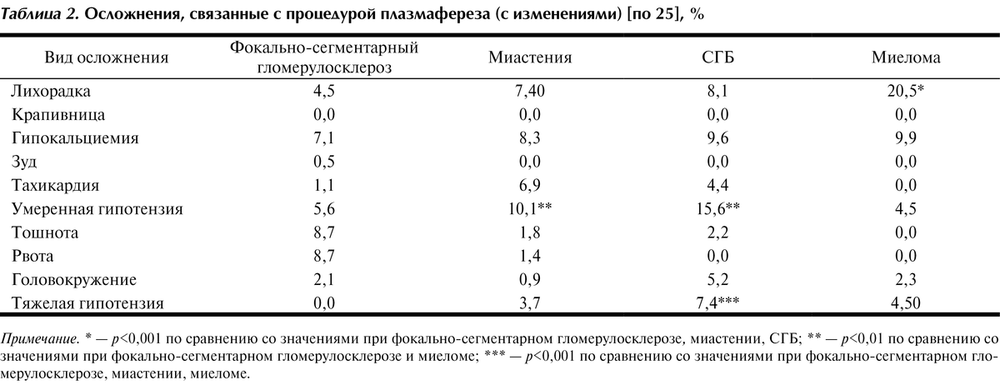
Затраты на терапию осложнений при проведении плазмафереза были рассчитаны с учетом данных указанных выше исследований и стоимости лечения одного случая нежелательного явления согласно тарифам на оплату медицинской помощи, оказываемой в стационарных условиях по законченным случаям лечения заболевания [26].
Кроме того, при расчете учитывались затраты на возмещение износа медицинского оборудования (амортизационные отчисления) и на время медицинского персонала.
Основную часть затрат при применении ВВИГ составили непосредственно затраты на препарат в курсовой дозе 2 г/кг [14]. Благодаря благоприятному профилю безопасности и удобству применения, частота осложнений была незначительной: головная боль возникала в 6,1% случаев, тошнота или рвота — в 5,6%, лихорадка — в 4,6%, локальные кожные реакции регистрировались в 4,6% случаев [27].
Результаты оценки прямых медицинских затрат показали их сопоставимость при проведении процедуры плазмафереза по сравнению с применением терапии ВВИГ препаратом привиджен (табл. 3). 
В ноябре 2016 г. в ГБУЗ ИКБ № 1 поступила девочка 7 лет с жалобами на боли в нижних конечностях, нарушение походки и изменение чувствительности в руках. Из анамнеза известно, что симптомы появились после интенсивной физической нагрузки в школе за 3 нед до обращения за медпомощью. Состояние пациентки прогрессивно ухудшалось: в первые 3 сут мама стала отмечать нарушение почерка, нарушение походки за счет слабости в ногах. В последующие 2 нед двигательные нарушения в ногах росли, выявлено снижение коленных сухожильных рефлексов, присоединилось онемение кистей.
При поступлении: состояние средней тяжести. В соматическом статусе без особенностей. Общемозговых знаков нет. Черепные нервы без патологии. Выявлялись симптомы натяжения, болезненность при пальпации по ходу нервных стволов на руках и ногах, снижение мышечного тонуса. С верхних конечностей вызывались только рефлексы m. biceps. Снижение мышечной силы в руках в проксимальных и дистальных отделах до 3 баллов, снижение поверхностной чувствительности по типу «перчаток». Сила в ногах снижена преимущественно в проксимальных отделах, более грубо в задней группе мышц бедра (до 3 баллов), сухожильные рефлексы не вызываются. Походка паретичная, из глубокого приседа встает только с использованием дополнительных приемов. Нарушений тактильной чувствительности и мышечно-суставного чувства в ногах нет. Нет нарушений функции тазовых органов. По данным исследования ЦСЖ выявлена белково-клеточная диссоциация.
Для исключения инфекционной природы заболевания проведено комплексное лабораторное обследование, в том числе серодиагностика крови и ЦСЖ с определением антител к иксодовому клещевому боррелиозу, вирусам простого герпеса 1-го и 2-го типов, V. zoster, Эпштейна—Барр, цитомегаловирусу, которая не выявила признаков активности указанных агентов.
При электронейромиографии (ЭНМГ) большеберцового нерва слева при поступлении (на 3-й неделе заболевания): при стимуляции в дистальной точке М-ответ псевдополифазный, увеличена латентность. Характеристика М-ответа (точка стимуляции — предплюсна): латентность 25,1 мс, длительность 16,1 мс, амплитуда 0,08 мВ (норма 3—10 мВ), отклонения амплитуды 97,7%, площадь 0,44 мВ/мс, расстояние стимуляциия—отведения 75 мм, стимуляция 100 мА, стимуляция 100 мкс. Скорость распространения возбуждения по моторным волокнам (точка стимуляции — предплюсна): время 25,1 мс, скорость 2,99 м/с (норма 50 м/с), отклонение скорости 94%, расстояние стимуляции—отведения 75 мм.
При стимуляции в проксимальной точке М-ответ не получен. При исследовании срединного нерва слева: М-ответ псевдополифазный, увеличена латентность, S-ответ получить не удалось.
Проведено УЗИ периферических нервов рук и ног: визуализированы срединные, локтевые нервы, нервы плечевого сплетения, седалищные, малоберцовые, большеберцовые нервы. По данным исследования отмечалось набухание нервных волокон: зафиксировано диффузное, симметричное увеличение площади их поперечного сечения. При продольном сканировании отмечалось чередование участков сужения и расширения с нечеткими контурами, что характерно для дизиммунной полинейропатии.
Анамнестические, клинические данные и результаты комплексного лабораторного обследования подтверждали предположение о СГБ, протекающем в форме острой воспалительной демиелинизирующей полирадикулонейропатии. В качестве патогенетической терапии была выбрана тактика введения ВВИГ из расчета курсовой дозы 2 г/кг за 5 дней.
На фоне проводимой терапии ВВИГ (препарат привиджен) уже на 5-й день лечения наметилась положительная динамика в виде нарастания двигательной активности и тонуса мышц конечностей, рисунок походки улучшился. Появилась возможность стоять на носках и пятках, короткое время стоять на одной ноге. В руках мышечный тонус приблизился к физиологическому, сила наросла до 4 баллов, появились сухожильные рефлексы с трехглавой мышцы. В ногах сила 4 балла, сохранялся сниженный мышечный тонус и негрубый радикулярный синдром. Выписана из стационара в удовлетворительном состоянии на 17-е сутки госпитализации. Рекомендованы курсы ЛФК.
В катамнезе через 2 мес после выписки: состояние удовлетворительное, активных жалоб нет. Чувствительных нарушений нет. Мышечная сила в руках не снижена, в ногах выросла до 5 баллов. Сухожильные рефлексы с рук вызываются, с ног отсутствуют. Увеличилась физическая активность: может стоять короткое время на одной ноге, пройти без поддержки более 10 шагов, самостоятельно подниматься по лестнице. При проведении контрольного ЭНМГ отмечается нарастание скорости распространения возбуждения, нарастание амплитуды и уменьшение латентности М-ответа. Характеристика М-ответа (точка стимуляции — предплюсна): латентность 7,7 мс, длительность 14 мс, амплитуда 2,16 мВ (норма 3—10 мВ), отклонения амплитуды 38,3%, площадь 11,4 мВ/мс, расстояние стимуляции—отведения 142 мм, стимуляция 62 мА, стимуляция 500 мкс. Скорость распространения возбуждения по моторным волокнам (точка стимуляции — предплюсна) 27,1 м/с (норма 40—60 м/с), время 2,46 мс (норма 2 мс).
Приведенный клинический случай демонстрирует типичную для СГБ клиническую картину с острым началом, быстрым достижением пика заболевания с выраженным двигательным дефицитом и хорошим ответом на терапию ВВИГ. Своевременная диагностика и правильная тактика патогенетической терапии имели ключевое значение и позволили остановить патологический процесс повреждения нервного волокна, а также создали предпосылки к полному восстановлению утраченных функций.
В рамках фармакоэкономического анализа было проведено сравнение прямых медицинских затрат на терапию пациентов детского возраста с СГБ с применением ВВИГ (привиджен) и плазмафереза. Оценка прямых медицинских затрат показала сопоставимость затрат на проведение сеансов плазмафереза по сравнению с терапией ВВИГ препаратом привиджен. Учитывая более благоприятный профиль безопасности ВВИГ по сравнению с плазмаферезом, применение препарата привиджен у пациентов детского возраста можно считать оправданным.
Приведенные данные позволят сотрудникам лечебных учреждений, в которых проходят лечение дети с СГБ, принимать более обоснованное решение относительно выбора тактики терапии.
Материал подготовлен при финансовой поддержке филиала ООО «Си Эс Эл Беринг Биотэрапис ГмбХ».
Авторы заявляют об отсутствии конфликта интересов.
*e-mail: armen2@mail.ru
Подтверждение e-mail
На test@yandex.ru отправлено письмо со ссылкой для подтверждения e-mail. Перейдите по ссылке из письма, чтобы завершить регистрацию на сайте.
Подтверждение e-mail
Мы используем файлы cооkies для улучшения работы сайта. Оставаясь на нашем сайте, вы соглашаетесь с условиями использования файлов cооkies. Чтобы ознакомиться с нашими Положениями о конфиденциальности и об использовании файлов cookie, нажмите здесь.